Как ответить: 24.8 г порошка светло‑зелёного цвета растворили в 78.4 г?
24.8 г порошка светло‑зелёного цвета растворили в 78.4 г раствора кислоты, широко используемой в промышленности. В ходе реакции выделилось 4.48 л бесцветного газа без запаха (н.у.) и образовался голубой раствор с массовой долей средней соли 33.9 %, масса которого составила 94.4 г.
Какой газ мог выделиться в ходе проводимой реакции?
Аргон
Гелий
Хлор
Углекислый газ
Водород
Сернистый газ
Сера
Найдите массовую долю кислоты в начальном растворе, учитывая, что вещества прореагировали полностью. Ответ выразите в процентах, округлите до целых.
Ответы (1)
"Страшная" на первый взгляд задача на поверку оказалась несложной. Если честно, то мысль о солях меди пришла мне в голову сразу после того, как я увидел упоминание о голубом растворе. Вероятно, речь шла о некоем популярном, широко известном металле, а среди таковых именно медь способна образовывать соли голубого и зелёного цвета (то, что по-вьетнамски назвали бы xanh, так как у вьетнамцев одно базовое слово и для голубого/синего, и для зелёного). Кстати, если я ничего не путаю, то соль CuCl₂ имеет зелёный цвет. А сульфат меди — как раз голубой. Что ещё могло образоваться растворимого? Ацетат меди имеет сине-зелёный цвет, что не идентично голубому. Есть смысл остановиться на сульфате. А значит, у нас была серная кислота. Она более чем широко применяется в промышленности!
К сожалению, изначально в своих рассуждениях я ошибся с типом соли. Я-то подумал, что это малахит (гидроксокарбонат меди(II)). Моя ошибка состояла в том, что, оказывается, малахит просто зелёный (даже ближе к тёмно-зелёному). А у нас порошок реагента светло-зелёный.
Итак, у нас была средняя соль — карбонат меди.
Но давайте придём к ней численным путём.
Понятно, что выделиться мог только углекислый газ!
[Почему? Сера — это не газ. Хлор имеет жёлто-зелёный цвет (а у нас газ бесцветный). Сернистый газ SO₂ обладает резким характерным запахом, а у нас по условию выделился газ без запаха. Гелий и аргон — благородные газы, они никак, ни при каких условиях не могут быть ни реагентами реакции, ни продуктами. Осталось исключить водород, но водород в основном выделяется при реакции кислот с металлами, но, на мой взгляд, не существует металлов зелёного цвета.]
Согласно закону Авогадро, количество вещества выделившегося газа однозначно определяется его объёмом. Давайте найдём количество вещества выделившегося углекислого газа:
ν(CO₂) = V(CO₂) : Vm(газов) = 4,48 л : 22,4 л/моль = 0,2 моль.
Будем молиться, чтобы все коэффициенты в нашей реакции равнялись единице — тогда количество вещества соли также равняется 0,2 моля. Попробуем найти молярную массу нашей соли:
M(соли) = m(соли) : ν(соли) = 24,8 г : 0,2 моль = 124 г/моль.
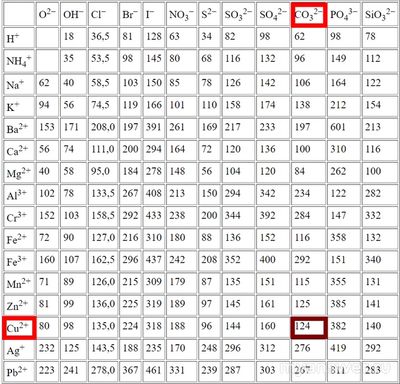
Здесь новое затруднение. Без таблицы подобрать химическую формулу сложно, но таблица молярных масс ряда распространённых неорганических веществ нас выручит (вероятно, я предполагаю, что на экзаменах и олимпиадах ею могут разрешить пользоваться).
Мы видим, что числу 124 соответствует средний карбонат меди(II). Его химическая формула — CuCO₃.
[Если бы числа́ 124 в таблице не оказалось, то это значит, что в реакции неравные коэффициенты. Тогда я бы бросился искать дольные и кратные величи́ны: искал бы чи́сла 248, 372, а также 62... К счастью, этого не понадобилось!]
Мы почти уверены, что была взята серная кислота, но если это действительно так, то образовался сульфат меди(II). И всё же проверим этот факт тоже численным способом!
m(CuSO₄) = m(р-ра CuSO₄) * ω(CuSO₄) : 100 % = 94,4 г * 33,9 % : 100 % = 32 г;
ν(CuSO₄) = m(CuSO₄) : M(CuSO₄) = 32 г : 160 г/моль = 0,2 моль = ν(CO₂). Всё верно, всё сходится!
Мы можем наконец-то записать наше полное уравнение химической реакции:
CuCO₃ + H₂SO₄ (разб.) = CuSO₄ + CO₂↑ + H₂O.
Теперь найти массовую долю серной кислоты в начальном растворе не составит большого труда.
ν(H₂SO₄) = ν(CO₂) = 0,2 моль;
m(H₂SO₄) = ν(H₂SO₄) * M(H₂SO₄) = 0,2 моль * 98 г/моль = 19,6 г;
ω(H₂SO₄) = m(H₂SO₄) : m(р-ра H₂SO₄) * 100 % = 19,6 : 78,4 г * 100 % = 25 %.
Всё правильно: кислота именно разбавленная. Концентрированная (96–98 %) нам не пригодилась бы. Между прочим, конц. серная к-та — это сильнейший окислитель, а теперь обратите внимание на вышеприведённое уравнение химической реакции: это не ОВР, ибо ни один элемент свою степень окисления не поменял!
Окончательные ответы: выделиться мог только углекислый газ. Для реакции была взята серная кислота, а её концентрация в растворе на момент самого начала реакции составляла ровно 25 %. Солью-реагентом был средний карбонат меди(II), а после реакции в растворе образовался сульфат меди(II).